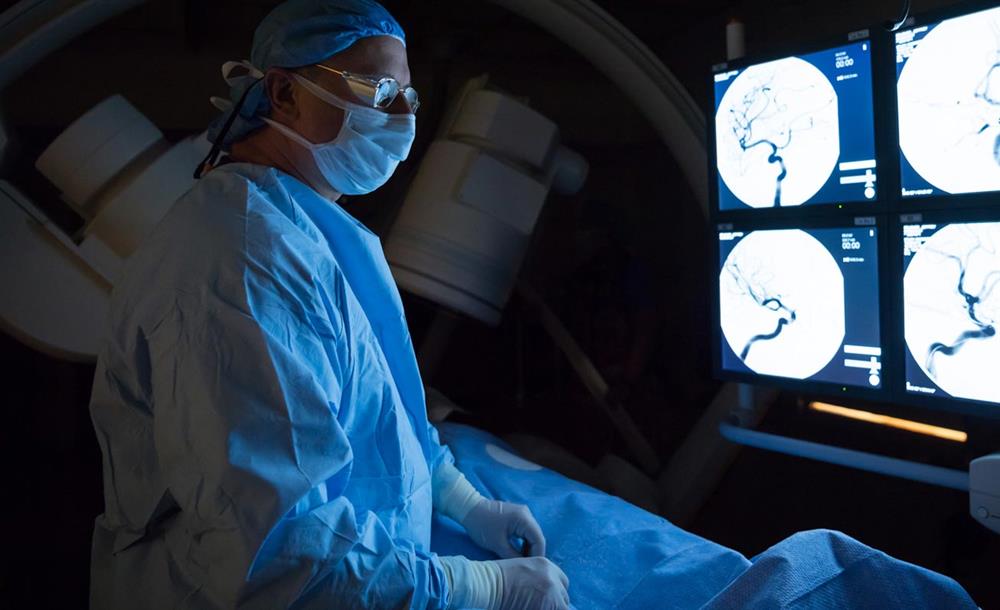
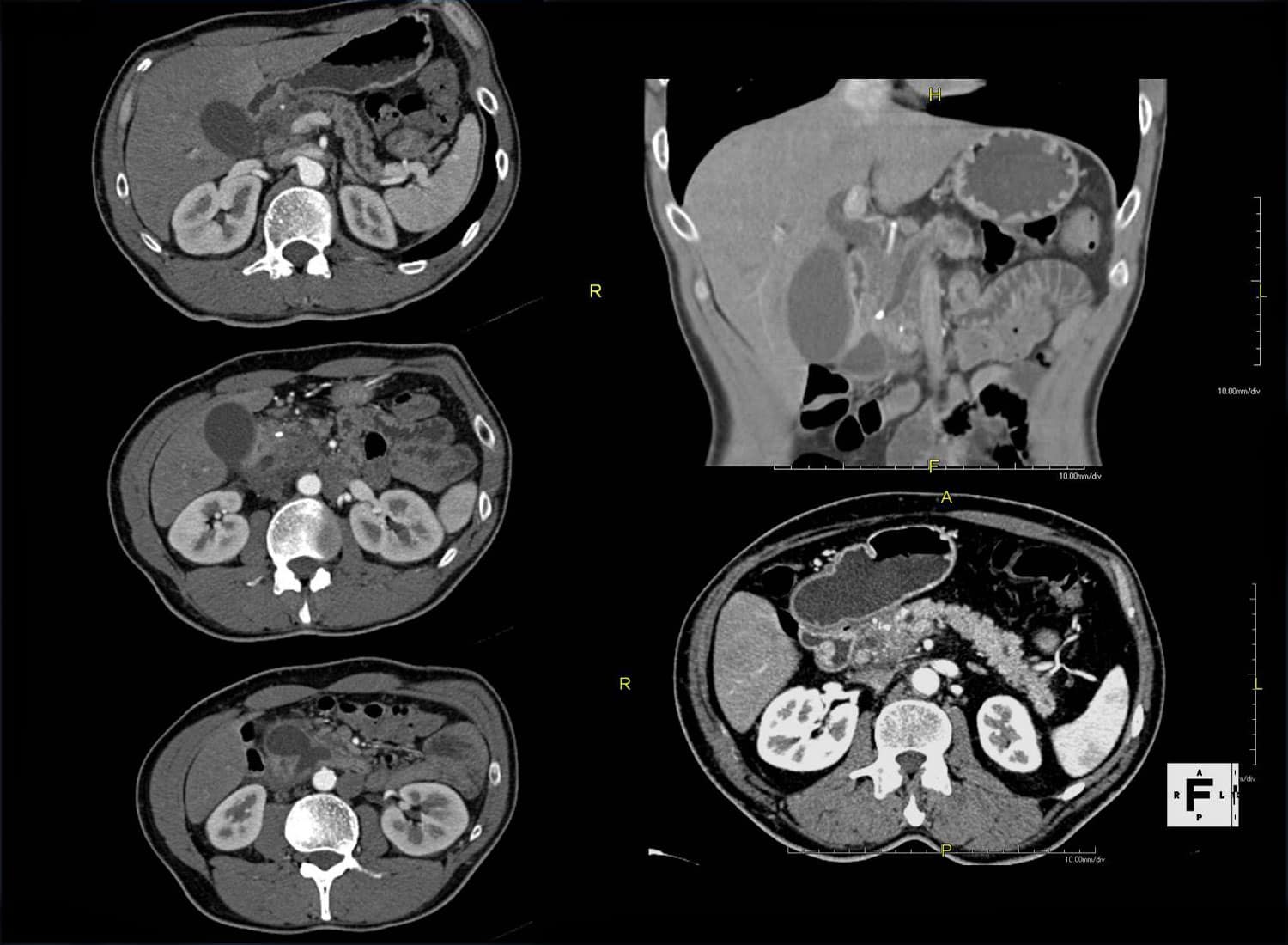
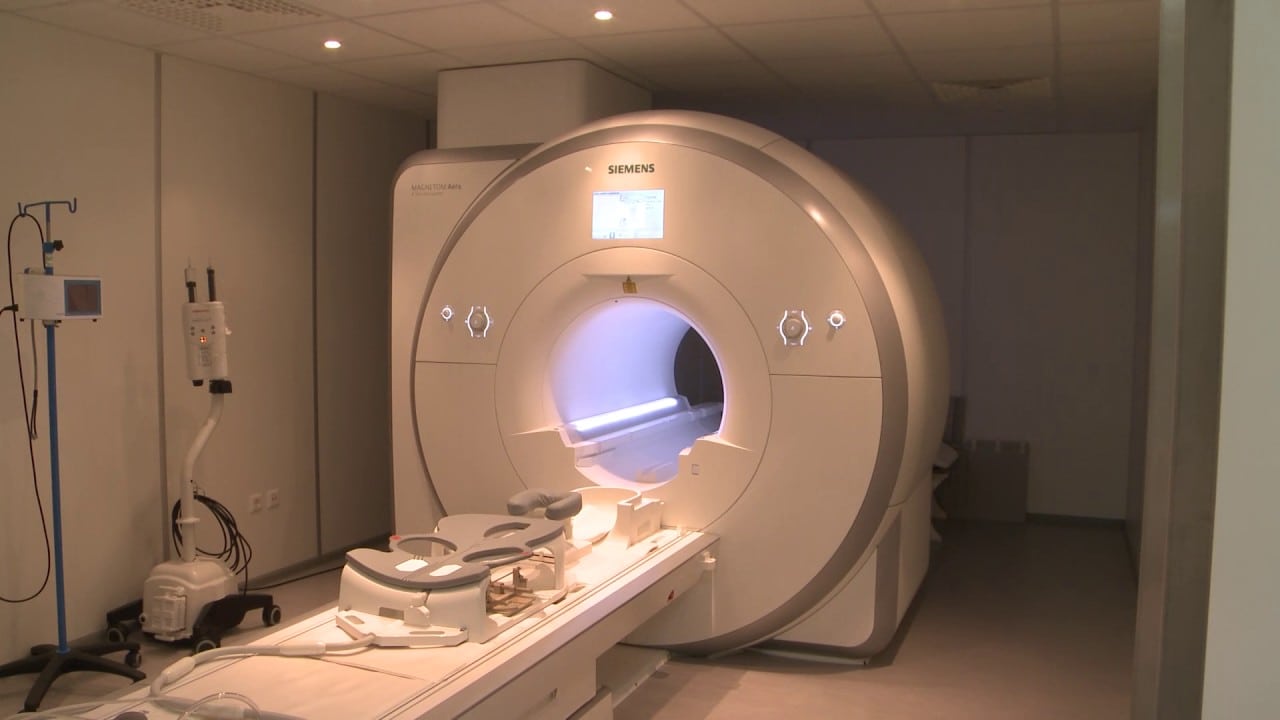
Врач-радиолог ЦКБ РАН Антон Кондаков рассказал медицинскому каналу «Медач» о том, кто такой врач-радиолог, вызывает ли лучевая диагностика мутации, вредны ли МРТ и КТ, а также заменит ли протонная терапия классическую нейрохирургию.

– С чем связана работа врача-радиолога?
– Работа врача-радиолога связана с радионуклидной диагностикой. Это моя первичная специализация, первичная область научных интересов. Мы проводим радионуклидные исследования, сцинтиграфическую, позитронно-эмиссионную томографию, совмещённую с компьютерной томографией, и фактически находимся на острие радионуклидной диагностики, на острие лучевой диагностики, изучая различные процессы, протекающие в человеческом организме.
Радионуклидная диагностика – это часть лучевой диагностики в целом, которая охватывает именно функциональные механизмы, циркуляцию различных метаболитов в организме человека, меченных радиоактивными атомами. Излучение, которое мы фиксируем, исходит из тела пациента и регистрируется внешним датчиком. В этом заключается основное отличие радионуклидной диагностики от компьютерно-томографических рентгеновских стандартных диагностических процедур, когда источник излучения находится вне тела человека.
– То есть, вы вводите радиоактивное вещество, и уже это вещество, циркулирующее в крови, компьютерная томография, магнитно-резонансная томография начинает оценивать?
– Не совсем так. Действительно, мы вводим меченое радиоактивное вещество. Самый простой пример – это, наверное, радиоактивный изотоп йода йод-131, который, циркулируя в крови, захватывается клетками, содержащими на своей поверхности натрий-йодный симпортер. Затем мы применяем специальное оборудование – однофотонный эмиссионный компьютерный томограф (может быть, более привычное его название – гамма-камера) или позитронно-эмиссионный томограф и регистрируем излучение. В отличие от обычного компьютерного томографа, у позитронно-эмиссионного томографа, у гамма-камеры, нет специального источника излучения. Это большой фотоаппарат на основе сцинтилляционных детекторов, в которых под воздействием ионизирующего излучения возникает свечение, регистрируемое, так скажем, электрической цепью. Затем мы видим на экране распределение вещества в организме человека. Этот достаточно точный количественный метод позволяет оценить нам, в зависимости от того, сколько препарата накопилось в каждом органе тела человека, его функциональную способность. В частности, для оценки функции щитовидной железы и узловых образований в ней используется радиоактивный йод, о котором уже говорилось выше. Чем больше накапливает его узловое образование в щитовидной железе, тем более оно функционально активно, тем большее количество гормонов производит. Тем выше его функция и степень влияния на уровень гормонов в крови. Учитывая полученные данные, врач-эндокринолог определяет дальнейшую тактику лечения. Автономные узлы, не подчиняющиеся командам гипофиза, не подчиняющиеся уровню ТТГ, необходимо лечить либо антитироидными препаратами, либо хирургически удалять. Узловые образования, которые не накапливают йод и не производят большого количества гормонов, можно оставить и длительно за ними наблюдать.
– Не приходится ли сталкиваться в работе с предубеждениями, с определёнными установками, с боязнью излучения со стороны пациентов?
– Конечно, периодически сталкиваемся. Бывает, что пациенты интересуются, не придётся ли им сжигать свою одежду после проведения нашего исследования. К сожалению, радиация – это всегда нечто стигматизованное, нечто опасное, загадочное. Здесь играют роль и когнитивные искажения человеческого сознания, которое способно переоценивать маленькие риски, а риски, связанные с диагностической радиацией – действительно, маленькие. Если сравнить дозы, которые пациент получает при радионуклидной диагностике, при сцинтиграфическом исследовании, то они сопоставимы с дозами, получаемыми при компьютерной томографии. Это вполне переносимые, толерантные дозы, с которыми организм легко справляется.
Но, к сожалению, у нас есть негативный опыт: все слышали об атомных станциях, о Чернобыльской аварии, которая произошла в 1986 году, и о других авариях. И радиация, в связи с этим, достаточно сильно стигматизована. Нормативные документы, которые сейчас существуют и описывают нормы радиационной безопасности, основные санитарные правила радиационной безопасности, основываются на стандартной линейной беспороговой модели. Она предполагает, что любая доза радиации вредна, и с увеличением дозы радиации в линейной степени возрастают и риски, с которыми она связана. Сейчас эта теория достаточно дискуссионна, существует ряд научных работ, которые её опровергают. Теория была основана на результатах исследований японских учёных, которые проводились в 1950-е годы и базировались на основе оценки количества опухолей у выживших после бомбардировок Херосимы и Нагасаки.
Сейчас, работая в области диагностической визуализации, мы располагаем результатами исследований, располагаем данными, что малые дозы – меньше 50 миллизивертов или 100 миллизивертов – не вызывают каких-то детерминированных эффектов. Это те дозы, с которыми человек может встретиться в быту. Такие дозы можно получить, например, в течение года прожив в провинции Рамсар в Иране – там, где естественный радиационный фон чрезвычайно высок. Любопытный факт, доказывающий, что существует уровень радиации, который человек может переносить без вреда для здоровья – это то, что в этой провинции частота онкологических заболеваний не выше, чем в соседних областях.
– Как вы пришли в специализацию, почему выбрали радиологию?
– Путь был долгим. Я из города Обнинск. Это город атомщиков, город первой атомной станции, город, связанный с радиацией. Это, наверное, и привело меня в конечном итоге на медико-биологический факультет, я окончил медицинскую биофизику и в качестве работы выбрал не научную деятельность, а склонился в сторону клиники. Прошёл ординатуру – сначала по классической рентгенологии, затем переподготовку по радиологии. В радионуклидной диагностике я начал работать в 2012 году.
– Как попадают пациенты к врачу-радиологу? Может ли человек обратиться без направления лечащего врача, по собственной инициативе?
– Законодательного документа, напрямую запрещающего человеку прийти, заключить договор и пройти исследование, не существует. Конечно, пациентов, которые обращаются к нам напрямую, подозревая у себя наличие какого-то новообразования, мы стараемся, в первую очередь, направить к онкологу, который проанализирует симптоматику и, возможно, предложит какие-то более дешёвые, более разумные методы диагностики. Возможно, врач проведёт классический скрининг на основные онкомаркеры и сможет убедить пациента, что ему наше исследование не нужно. Тем не менее, периодически бывает так, что пациенты записываются и приходят. Мы предупреждаем их о том, что лучевая нагрузка всё равно существует. Рассказываем о рисках, и порой человек приходит к мысли, что ему, наверное, не стоит делать дорогое и потенциально опасное исследование без наличия каких-либо существенных симптомов. Но периодически в электронной системе всё же появляются три пациента с одинаковыми фамилиями – скорее всего, отец, мать и сын, которые записались на ПЭТ.
– Можете вспомнить какие-то нелепые случаи из практики?
– Периодически случаются, хотя я бы не сказал, что они нелепые. Всё-таки большинство пациентов – это пациенты с онкологическими заболеваниями. Они уже достаточно подготовлены своими лечащими врачами к исследованиям, причём подготовлены не только с точки зрения физиологической, но и с точки зрения психологической. Они знают, как проходит исследование, тем более, что мы их при встрече обязательно об этом предупреждаем. И всё же периодически случаются курьёзы.
Например, был случай, когда пациентка, страдающая клаустрофобией в лёгкой форме (то есть, по большому счёту, нахождение в томографическом аппарате она перенести может) взяла и выбралась из томографа. Стояла рядышком. Медсестра в этот момент отвернулась и не обратила внимания, что пациентка покинула гентри. А ведь это непросто сделать! Те, кто проходил компьютерную томографию, МРТ, знают, что вылезти оттуда не так легко. А она почему-то решила, что исследование закончилось. Так она нам объяснила свои действия. Пришлось её заново уложить, пересканировать, приставив рядышком медсестру, чтобы она её держала за ручку и гладила. Забавная ситуация. Иногда случаются казусы с подготовкой пациентов, которые забывают выложить из кармана ключ и вспоминают об этом в середине сканирования. И это несмотря на то, что, как правило, мы стараемся заранее убедиться, что металлические предметы не мешают исследованию, уточняем у пациента, всё ли он выложил из карманов.
Бывают ситуации, когда пациенты не очень хорошо представляют себе суть исследования и начинают после введения радиоактивного препарата – а обычно после этого прикладывается ватка, накладывается бинт – берут в руки эту ватку и начинают себя тереть, размазывая радиоактивный препарат по коже. Такие случаи тоже бывают, и мы с ними успешно справляемся.
– Вы работаете в центральной клинической больницы РАН. В какой-то ещё больнице проводятся ПЭТ-исследования?
– Да, конечно. Таких больниц много, но, как обычно, недостаточно. По рекомендации международных онкологических обществ для обеспечения пациентов достаточным количеством ПЭТ-аппаратов необходимо иметь один позитронно-эмиссионный томограф на миллион населения. В Москве эта норма практически выполняется: здесь работает порядка 15-20 ПЭТ-центров, они покрывают необходимыми исследованиями всё население Москвы. Но на территории России суммарно количество таких центров не дотягивает до 50. Их около 40. Как мне известно, они развиваются, строятся новые центры, это радует. Растёт потребность и во врачах-рентгенологах, которые будут оценивать компьютерно-томографическую составляющую изображения, и потребность во врачах-радиологах, которые оценивают радионуклидное распределение фтордизоксиглюкозы в организме человека. Фтордезоксиглюкоза – это самая рабочая лошадка в области радионуклидной диагностики.
– А зарубежные клиники соответствуют рекомендациям всемирных организаций? Или там тоже есть недостаток в радионуклидных исследованиях?
– Зарубеж – понятие широкое. Всё по-разному. В Германии, например, на 70-80 миллионов человек приходится порядка 89 томографов, 89 ПЭТ-центров. Там очень хорошо организована система доставки препаратов. В позитронно-эмиссионной томографии используются короткоживущие препараты, они должны либо синтезироваться на месте, либо доставляться на какое-то небольшое расстояние. В Германии отлично организована эта система. В США, с которыми мы периодически сравниваем свою страну, порядка двух тысяч ПЭТ-центров на 300 миллионов населения, то есть, они сильно перевыполняют норму. Проблем у них с этим нет. Проблемы возникают с сцинтиграфическими исследованиями, с препаратами технеция. У нас в этом плане всё довольно спокойно и стабильно, потому что работает несколько реакторов на территории страны, где производится предшественник технеция – молибден-99. Пакуется генератор, отвозится в больницу, и этот генератор работает в больнице примерно неделю или две, выдавая технеций для проведения радионуклидных исследований.
В США это большая проблема, там достаточно часто случаются прекращения поставок. Они связаны с тем, что большинство реакторов, которые производят молибден для генераторов, уже достаточно старые. Они периодически выключаются. В Канаде не так давно заглушили такой реактор. Им приходится молибден привозить из других стран. Исторически сложилось, что с ядерными технологиями в России всё довольно неплохо. Забавным фактом можно назвать и то, что генератор рубидия – другого препарата для ПЭТ, который используется для оценки перфузии миокарда и для точного расчёта скорости миокардиального кровотока – производится под маркой компании Bracco. Это американская компания, но сама колонка и сами радионуклиды производятся у нас – в Объединённом институте ядерных исследований. Так что мы вносим вклад в американское здравоохранение.
– Вы описали достаточно длинный путь прихода в практическую часть радиологии. Каждый ли специалист, который хочет заняться радиологией, должен его пройти? Или есть другие варианты? Как стать врачом-радиологом?
– Лучше всего начинать этот путь именно с классической рентгенологии. Если обойти эту стадию и получить сразу специализацию радиолога после ординатуры (это сделать, в принципе, можно), теряются основные базовые знания по рентгенологии, и врач становится очень узконаправленным специалистом. Это ему мешает, потому что все томографы, в том числе, и позитронно-эмиссионный, связаны с компьютерным томографом. Они всегда работают в связке, и базовая рентгенология обязательно нужна. Кроме того, если человек получает специализацию радиолога изначально после ординатуры, он не может потом получить образование рентгенолога в связи с особенностями российского законодательства.
Если мы вернёмся к разговору про образование, у нас достаточно короткая ординатура. Два года – это катастрофически мало. Хотелось бы лет пять стандартного обучения в ординатуре, примерно так, как это происходит в Европе. Причём там это происходит не на одной базе, а на многих базах: молодые специалисты переезжают из центра в центр. Они могут поучиться в пределах Евросоюза в Швеции, Германии, Австрии. Могут сопоставить опыты этих центров, изучить в лучших центрах лучшие практики. Где-то они занимаются кардиологической практикой, кардиологической специализацией, обучаются, например, коронарографии. Затем, через несколько месяцев, полгода, год, переезжают в другой центр, изучают абдоминальную визуализацию кишечника, печени. Сопоставляют между собой возможности различных методов исследования, обязательно описывают эти исследования. И всё это приводит к формированию законченного специалиста, образованного специалиста, который может работать фактически в любой области, у которого есть знания по всем особенностям, по всем аспектам лучевой диагностики. Такой специалист без труда находит себе работу. И он может, работая, сопоставлять и выбирать правильные методы исследования для каждого конкретного пациента.
– Существуют ли программы обмена для тех, кто хочет обучаться радиологии за рубежом? Действуют ли какие-то договорные программы между нашими медицинскими университетами и зарубежными?
– Сказать, что такого не существует, не могу. Есть замечательная Европейская Школа Радиологии (ESOR), которая предлагает такие программы. Правда, они больше рассчитаны не на студентов, а на ординаторов, на молодых врачей. Эти программы позволяют пройти практику в зарубежных центрах. ESOR предлагает гранты, которые, как правило, спонсируются различными организациями, производящими препараты, оборудование, контрастные вещества. Кроме того, сейчас в Европейском обществе радиологии и Европейском обществе гибридной визуализации есть специальные программы по относительно бесплатному грантовому обучению в форме лекций. По-моему, стоимость двухдневного цикла лекций по какой-либо специальной проблеме составляет 200-300 евро.
– В чём будущее радиологии? Какие сейчас проводятся исследования, которые завтра помогут в излечении пациентов от онкологии?
– Лечить мы вряд ли научимся. А вот диагностировать получается уже гораздо раньше и лучше. За последние 20-30 лет диагностика шагнула далеко вперед и увеличила свои возможности. Выявляется больше заболеваний на ранних стадиях, их пытаются лечить лучшими методами. Но есть свои особенности. На острие радионуклидной визуализации находятся, в первую очередь, новые препараты для оценки опухолей. Я уже говорил, что главной рабочей лошадкой у нас является фтордезоксиглюкоза. Она накапливается в злокачественных образованиях, поскольку у них достаточно высокая метаболическая активность, высокая утилизация глюкозы. Тем не менее, этот метод не всегда хорош – например, при исследовании головного мозга, где физиологически повышен захват глюкозы. Поэтому для головного мозга разрабатывают специальные препараты – такие, как алониноремичный метиламин. Это аминокислота. Аминокислоты мало используются головным мозгом, метаболическая активность низкая. А вот скорость строительства белков в опухолевых клетках достаточно высокая, и они очень активно захватывают эти препараты.
Кроме того, можно сказать о фтортимидине, который также захватывается головным мозгом. По поводу лечения неонкологических заболеваний хочу сказать. Многие антипсихотические препараты, которые используются в лечении нервных заболеваний, психических расстройств, проходят исследование с использование ПЭТ-технологий. ПЭТ может пометить любой фармацевтический препарат при помощи атома углерода. Углерод входит фактически во все органические молекулы и простым метилированием или чуть более сложными методами можно изучить его распределение, изучить его активность, связанность с рецепторами и увидеть, где эти рецепторы у человека распределены.
Это большая работа, которая сейчас проводится во многих научных центрах, как правило, за рубежом, и она направлена на визуализацию тех или иных рецепторов в головном мозге. Сейчас активно развиваются гибридные технологии визуализации, связанные с комбинацией различных методов. Можно скомбинировать КТ и УЗИ, можно скомбинировать ПЭТ и КТ, можно скомбинировать ПЭТ и МРТ. Аппараты ПЭТ-МРТ стоят достаточно дорого и используются ограниченно – как правило, для научных исследований. Тем не менее, они позволяют получать гораздо больше информации. Магнитно-резонансная томография, в частности, позволяет получить достаточно много информации о состоянии структур головного мозга, о наличии в них каких-то морфологических изменений. Мы добавляем сюда ПЭТ с мечеными химическими соединениями, которые отражают распределение рецепторов, и получаем функциональную картину. Мы можем провести функциональную ПЭТ-МРТ, которая на основании изменения уровня кислорода в крови построит карту распределения активности в головном мозге, и на это наложить картинку распределения глюкозы в тот же самый момент при выполнении тех же самых задач. Мы можем сопоставить картинки между собой и оценить, как головной мозг работает, как он поглощает глюкозу, и соответствует ли это поглощению кислорода.
– Помогает ли описанная технология визуализировать и как-то диагностировать на ранних этапах, например, болезнь Альцгеймера?
– Да, помогает. И однофотонная эмиссионная компьютерная томография, связанная с технецием, и исследования с фтордизоксиглюкозой дают распределение метаболической активности глюкозы в головном мозге или перфузии головного мозга (они, как правило, между собой примерно взаимосвязаны). И на этом фоне мы можем видеть изменения в головном мозге, которые приводят при болезни Альцгеймера к специфическому снижению метаболизма глюкозы в теменных и височных долях. И при других видах деменции мы видим изменения. При лобно-височной деменции, соответственно, страдают лобные и височные доли. При болезни Паркинсона есть свои особенности: там тоже есть нейродегенерация, есть связанные с этим дементные расстройства. Здесь для диагностики мы отказываемся от фтордизоксиглюкозы и переходим к более специфичным методам: пытаемся визуализировать метаболизм дофамина в головном мозге, количество транспортеров дофаминовых, и их уменьшение будет склонять нас к тому или иному диагнозу.
По поводу развивающихся технологий: при болезни Альцгеймера достаточно активно в последние десятилетия исследуются препараты, которые позволяют нам увидеть амилоид. Это меченный фтором или углеродом краситель амилоидный. Есть несколько разных форматов этих красителей от разных производителей. Они накапливаются в головном мозге, связываются с изменёнными отложениями амилоида и позволяют визуализировать его распределение в головном мозге. У здоровых людей амилоида практически нет. У пациентов с болезнью Альцгеймера мы увидим характерные изменения в височных, теменных и – на поздних стадиях – лобных долях: там большие отложения амилоида. Однако и тут возникает некоторая неоднозначность: когда эти исследования начали проводиться, для них брали, в том числе, и когнитивно сохранных пациентов, и выяснилось, что у таких пациентов – примерно у каждого пятого – есть отложения амилоида, характерные для болезни Альцгеймера. Поэтому пошли новые исследования, которые включали в себя определение более специфичных маркеров. Для болезни Альцгеймера это нейрофибриллярные клубки, которые также возможно визуализировать при помощи меченых красителей. Сейчас технология с применением амилоидных красителей используется в редких достаточно случаях ранней болезни Альцгеймера, которая возникает у относительно молодых людей – в 40-50 лет. И когда необходимо определиться, всё-таки это болезнь Альцгеймера или нет, мы прибегаем к визуализации амилоида.
– Может ли технология нейровизуализации при помощи радионуклидов использоваться при диагностике не только болезни Альцгеймера, но и шизофрении, депрессии и других нервных расстройств?
– Может, и в этом большой плюс радионуклидной диагностики по сравнению с остальными методами исследования. Если мы будем говорить о депрессии (а её причина, мы знаем, в уровне серотонина), мы можем взять предшественник серотонина, пометить его углеродом и посмотреть, нарушен ли синтез серотонина. Это первая стадия. Если синтез не нарушен, переходим ко второй стадии – стадии рецепторов. Мы берём меченый серотонин или меченые аналоги серотонина, вводим внутривенно пациенту и смотрим, есть ли нарушения в самих рецепторах. Таким образом, мы проводим исследование на разных стадиях, на разных этапах, и на каждом этапе у каждого пациента мы можем исследовать причину нарушения, причину депрессии. Или вообще выявить, что она имеет место быть. Но это, как правило, большие научные исследования, потому что синтез таких препаратов на поток не поставлен. Этим занимаются крупные университетские центры, которые специализируются на лечении депрессии и лечении других заболеваний, связанных с депрессией. У них есть специальные методы лечения этих заболеваний. Существуют радиофармпрепараты, которые используются при диагностике биполярных расстройств. То есть, радионуклидная диагностика в лечении нервных расстройств применяется, но здесь, мне кажется, играет большую роль подход врача, который наблюдает пациента, определяет дальнейшую тактику его лечения. Дело в том, что нейропсихологи, психологи, психиатры, которые ведут пациента, не всегда понимают, зачем это нужно. Мы пытаемся объяснить и, в частности, у нас наладилась работа с пациентами с болезнью Альцгеймера. Неврологи ощутили, как могут наши методы помочь при дифференциации сложно различимых между собой лобно-височной деменции и болезни Альцгеймера. Поток таких пациентов у нас небольшой, но стабильно присутствующий.
– Существуют ли курсы по радиологии для врачей из других специальностей?
– Как правило, это работает больше на уровне личных контактов, личного общения между врачами, например, на профильных мероприятиях. У нас есть такая выставка здравоохранения – там между собой врачи общаются. Есть конгресс идеологии, который проходит традиционно в конце мая. Там тоже врачи общаются. Но, честно говоря, я не встречался со специализированными курсами. Сейчас есть замечательный портал по непрерывному медицинскому образованию. Я видел там ряд образовательных материалов, посвящённых радионуклидной диагностике, в частности, материал по диагностике ишемической болезни сердца, который был ориентирован не только на врачей-радиологов, но и на врачей-терапевтов, кардиологов, которые с этой методикой работают. И, судя по увеличивающемуся количеству запросов, работают достаточно активно.
– Сейчас на слуху тема телемедицины. Раз есть достаточное количество томографов на территории Москвы, можно ли как-то настроить отдалённую связь с нашими районами, с другими частями страны. Можно ли перевести эту работу в рамки телемедицины?
– Конечно. С 1 января 2018 года вступил в силу закон о телемедицине, который позволяет нам каким-то образом структурировать эту деятельность. Но и до вступления закона в силу были случаи, когда рентгенологи давали, как правило, второе мнение по уже описанному исследованию. В принципе, врачи любой больницы, в которой проводятся рентгенологические или радиологические исследования, обладают возможностью получить диск с информацией от пациента, посмотреть, провести анализ. Такая система достаточно эффективно работает за рубежом. Некоторые американские рентгенологи, радиологи, судя по рассказам, не выходят иногда из дома и очень удобно работают, общаясь с больницей только на основании пересылаемых исследований. Это не всегда хорошо, я думаю, потому что иногда нужно подойти к пациенту, что-то у него спросить, уточнить, посмотреть на него, оценить размер щитовидной железы визуально, пальпировать, поговорить с пациентом.
Большой спрос у пациентов на общение с врачами-рентгенологами, врачами-радиологами – люди хотят не просто получить бумажку с заключением, но и услышать мнение врача. Поэтому для нас такая зарубежная практика непривычна. В тех учреждениях, где я был, обязательно есть какой-то контакт врача, проводившего исследование, подготовившего заключение, с пациентом. В зарубежных странах, где рентгенолог напрямую не контактирует с пациентом, отправляя результаты лечащему врачу, результаты интерпретирует уже лечащий врач. Лечащий врач сообщает их пациенту. И эта технология тоже правильная. Мне кажется, пациенту всё-таки разумно получать оба мнения: и рентгенолога, и лечащего врача. Ну, а телемедицина, действительно, существует, и существуют различные производители серверов, на которых может храниться информация, различных систем архивации данных.
– Что можно сказать о мобильных установках? Существует ли возможность их использования?
– Да, такое возможно, с учётом, конечно, строгих правил работы с источниками ионизирующего излучения. Это касается не только открытых источников, которые мы используем в радионуклидной диагностике, но и рентгеновских аппаратов. Аппарат должен быть достаточно защищённым, пациент и окружающие люди не должны подвергаться высокому излучению. На базе фургонов, пикапов, других крупных машин можно установить любой томограф. Создаются, например, мобильные установки для быстрой диагностики инсульта. В этом случае КТ-аппарат встроен прямо в кузов машины, которая используется как “скорая помощь”. Пациента с инсультом кладут прямо в томограф в этой машине и, пока он едет до госпиталя, проводят компьютерную томографию, исключают геморрагическую природу инсульта. Если это не геморрагический, а ишемический инсульт, мы применяем стандартную технологию – тканевой активатор плазминогена, который вводится внутривенно пациенту.
Так мы стараемся соблюдать правило золотого часа, которое нам всем известно из курса неврологии – чем быстрее начато лечение, тем меньше выраженность ишемии, тем меньше пострадает мозг. Этот метод тоже порой критикуется, работает не всегда как надо, тем не менее, такие “скорые помощи” для пациентов с инсультами могут использоваться. Наверное, они стоят довольно дорого, так как требуется крупногабаритная машина под компьютерный томограф.
Стоит сказать, что и радионуклидная диагностика тут не отстаёт: существует возможность поставить ускорители частиц на шасси какой-нибудь машины, этот ускоритель продуцирует радиоактивное вещество, которое готовится тут же и вводится пациенту во второй машине, где стоит томограф. Прямо на месте. На ходу это сделать не получится, поскольку это требует подведения высокомощностных кабелей электрических. Речь идёт о больших энергетических затратах, аккумулятор сразу сядет, не выдержит такой нагрузки. Но подобные решения существуют и могут применяться, когда есть, например, отдалённая больница, и можно эти фургоны подогнать, поставить рядом, запитать от стационарной сети и провести исследование жителям отдалённого города или посёлка. Не сказать, что это технология новая: я ещё из своей молодости помню, что приезжал кузов со стоящей внутри флюорографической установкой, где проводили исследования и отправляли их результаты врачу. Но эта технология в наши дни совершенствуется.
– Что лучше использовать для обследования головного мозга: КТ или МРТ?
– Это очень сложный вопрос, потому что у каждого пациента есть свои особенности. Заболевания разные, и от этого зависит выбор метода диагностики. В случае, когда речь идёт об экстренной диагностике, метод КТ, как правило, более дёшев, доступен и быстр. Мы уже говорили про инсульты. Так вот, при дифференциальной диагностике инсультов – для исключения геморрагического поражения – быстрым способом является компьютерная томография. В случае ишемического инсульта она позволяет выявлять малые признаки инсульта на ранних стадиях, видя которые, мы можем этот диагноз установить, сопоставить с клиническими проявлениями и начать лечение в течение так называемого золотого часа. Однако если у пациента что-то более необычное – опухоли головного мозга, метастазы в мозге, рассеянный склероз – здесь магнитно-резонансная томография играет гораздо большую роль. Она отражает распределение молекул воды, их окружение, позволяет характеризовать плотность клеток, находящихся внутри образования, позволяет увидеть, есть ли вокруг отёк или нет, с гораздо большей точностью разрешения, чем компьютерная томография.
– Многие считают, что МРТ так же вредна, как КТ. Так ли это?
– МРТ не вредна с точки зрения ионизирующей радиации. Никакой ионизирующей радиации там нет. Есть обычные радиоволны и большой магнит. Негативное воздействие магнитных волн на человека никогда и никем не было доказано. Человек постоянно живёт в магнитном поле. Радиоволны МРТ сопоставимы с радиоволнами, на которых вещают радиостанции. Вы пользуетесь наушниками, слушаете радио в автомобиле, приезжаете к бабушке на дачу – там стоит длинноволновый приёмник, который ловит радио Ватикана каждый вечер с 10 до 11. То есть, мы живём в окружении радиоволн, в окружении электромагнитных волн. Негативного влияния МРТ в этом плане не оказывает.
Есть, разумеется, большое количество противопоказаний, связанных с имплантируемыми кардиостимуляторами. Они не способны работать в сильных магнитных полях, могут возникнуть их сбои, и это потенциально фатально для пациента. В этих случаях нам приходится избегать МРТ и переходить на КТ, хотя сейчас разрабатываются совместимые устройства. Правда, такие устройства не предназначены для визуализации области грудной клетки. Есть противопоказания, связанные с ферромагнитными протезами, аппаратами, установленными в организме ещё до появления МРТ, в 1970-1980-е годы: какие-то клипсы в головном мозге неизвестного характера. Такой протез мы можем обнаружить при помощи металлодетектора и отказать пациенту в исследовании. С клипсами в головном мозге вообще достаточно сложно, поэтому врачи запрашивают полную информацию об их происхождении, желательно с выпиской и составом, чтобы можно было их обнаружить и понять, как они будут вести себя в условиях сильного магнитного поля. Их может и сорвать, и подвинуть, и нагреть. Ничего хорошего мозгу это не принесёт. Для пациентов с клаустрофобией тоже выбор, как правило, делается в пользу КТ, потому что магнитно-резонансный томограф закрытого типа выгладит как труба. Американские радиологи называют его “пончик смерти”. Пациенты его достаточно часто боятся. Иногда этот страх необоснован, его трудно контролировать, и даже если пациенты не выскакивают из томографа и не кричат в нём, они начинают шевелиться. Дети, как правило, беспокойно себя ведут. Приходится седацию делать в этих случаях. Но важно понимать, что это ограничивает применение МРТ для исследования головного мозга, потому что седация влияет на уровень мозговой активности и обмен кислородом в головном мозге. Нужно каким-то образом либо договариваться с ребёнком, либо отказываться от этого исследования и переходить к другим видам исследования. КТ чувствительна к движениям пациента, но не настолько критично, как МРТ, в этом плане с КТ проще. И исследование проходит очень быстро. Сканирование всего тела занимает порядка 10-12 секунд на компьютерном томографе, который работает вместе с ПЭТ.
– Стимуляция мозга при помощи лучевой терапии – насколько это реальная возможность? Можно ли улучшить работу мозга, используя лучевую терапию?
– Лучевая терапия использует достаточно высокие уровни энергии излучения. Они, как правило, оказывают поражающий, а не стимулирующий эффект. В последнее время широко обсуждается при лечении опухолей головного мозга риск радиационно-индуцированной деменции. Это спорный вопрос: не всегда понятно, то ли такая деменция вызвана радиацией, то ли воздействием опухолей, то ли химиотерапией. Множество факторов не позволяют однозначно дать ответ на этот вопрос. Но возможно именно поражающее действие излучения. Однако, если мы посмотрим на ряд исследований, которые касаются теории положительного действия ионизирующего излучения, теорию радиационного гормезиса, то там говорится, что при низких диагностических дозах изучения (пять-десять-пятнадцать миллизивертов) организм в целом повышает сопротивляемость. И вообще, это действует и как иммуномодулятор, и как противоопухолевый фактор. Однако результаты таких исследований тоже не всегда однородны, не всегда их можно сопоставить между собой. И теория радиационного гормезиса остаётся на сегодняшний день всего лишь одной из теорий – наряду с теориями, которые говорят о том, что радиация всё-таки приносит вред.
– Вызывает ли лучевая диагностика мутации?
– Нет, мутации происходят далеко не так быстро. Мутагенный эффект радиации достаточно известен, является одним из побочных эффектов лучевого лечения, но речь идёт о небольших мутациях – скажем, об образовании пятна на коже. Оно возникает, потому что часть клеток, через которые проходил пучок излучения, получила мутацию, которая, например, способствует выработке определённого пигмента или, наоборот, депигментации. Эти мутации не всегда обнаруживаются.
– О протонной терапии говорят как о будущем в лечении онкозаболеваний, заболеваний нервной системы. Что Вы можете сказать об этом?
– Протонная терапия, в отличие от стандартных методов лечения, которые используются сейчас (гамма-терапии или терапии высокими энергиями линейных ускорителей) обладает замечательным эффектом, который называется пик Брэгга. Распределение гамма-излучения или тормозного излучения высокой энергии в теле человека устроено таким образом, что максимум приходится на кожу и потом происходит убывание, и для подведения дозы к глубоко лежащей опухоли нам потребуется несколько пучков излучения сопоставить друг с другом, направить друг на друга так, чтобы они пересекались и в опухоли создавали высокую дозу для её уничтожения. При этом окружающие ткани тоже получают достаточно высокую дозу. Чтобы этого избежать, стали придумывать различные установки. Наверное, самые известные – это гамма-нож и кибер-нож. В гамма-ноже источников излучения много, и они точечные. В кибер-ноже используется линейный ускоритель, который постоянно двигается, и из разных проекций облучает опухоль, уничтожая её таким образом. В протонной терапии распределение максимального поражающего эффекта, распределение ионизации отличается от описанных выше методов: максимум ионизации лежит в глубине ткани, и мы глубину этого максимума ионизации можем регулировать, регулируя энергию протонного излучения.
Таким образом, мы можем подводить прямо к самой опухоли максимум, сообщая минимальную дозу тем тканям, через которые прошёл пучок излучения и практически нулевую дозу тканям, лежащим за этим пучком, за этим пиком излучения. Это большой плюс, потому что это позволяет сохранять здоровые ткани неповреждёнными. Это очень важно в лечении головного мозга: в этом случае у нас нет “лишней” ткани, которою мы можем спокойно облучить, и от этого ничего не будет, как, например, в случае с печенью или с лёгкими. В головном мозге нет “лишней” ткани. Это ограничивает работу и хирургов, и нейрохирургов, и лучевых терапевтов. Протонная терапия в сохранении здоровых тканей очень помогает. Сейчас, к сожалению, количество центров протонной терапии не так велико, метод достаточно дорогостоящий, трудоёмкий, энергоёмкий.
Здесь большую роль играют медицинские физики и физики-дозиметристы, которые рассчитывают распределение протонов в ткани в зависимости от энергии, вместе с врачом участвуют в планировании такого лечения. Важно обеспечить неподвижность пациента и очень точное наведение пучка именно на опухолевый очаг, на образование, которое хотим вылечить. Это требует специальной подготовки, вероятно, поэтому количество таких центров не так велико. Во всём мире их порядка 70-80. Чаще всего они ассоциированы с крупными городами, связанными с физическими излучениями. Если мы говорим о Японии, это центр в городе Чиба, который длительное время уже работает. Японцы в этом плане являются одними из лидирующих наций. Если говорим о России, то эти установки расположены у нас в Обнинске, в городе Протвино (это города атомщиков) и в институте ядерных исследований. Даже в Москве, насколько я знаю, таких установок нет. Только за пределами МКАД.
– То есть, по сути, этот метод может заменить нам классическую нейрохирургию головного мозга, которая является достаточно повреждающей, если говорить о глубоко расположенных опухолях?
– Технически – да. Конечно, никто не может дать стопроцентной гарантии. Существуют опухоли, которые характеризуются сильным инфильтративным ростом в критически важные структуры, и в этом случае нам придётся всё-таки повреждать эти критически важные структуры. Если мы говорим о головном мозге, такой структурой, является, как правило, аппарат оптических нервов, зрительный перекрест, который очень чувствителен к радиации, и при достаточно высоких подведённых дозах облучения у человека может возникнуть слепота. Это один из ограничивающих факторов в радиотерапевтическом лечении опухолей головного мозга. В таких случаях приходится комбинировать методы. На сегодняшний день стандартными всё-таки являются именно хирургические операции: в случае низкозлокачественных опухолей проводится сама операция и затем ведётся динамическое наблюдение до появления рецидива. Если рецидив всё-таки возникает, то в этом случае врачи могут привлекать лучевую терапию в качестве вспомогательной методики. Либо же лучевая терапия сразу используется как стандартная вспомогательная методика. Так происходит в случае с высокозлокачественными опухолями головного мозга, такими как глиобластома, когда стараются сделать максимально безопасную резекцию, однако участки опухолевого роста всё равно остаются где-то в теле человека, в головном мозге. В этом случае комбинация химиотерапевтического лечения и лучевой терапии позволяет получить положительный эффект у пациентов, увеличить продолжительность жизни. К сожалению, в целом прогноз при этой опухоли неблагоприятный, и речь идёт, как правило, об увеличении медианы выживаемости на 2-4 месяца. Тем не менее, эти технологии применяются.
– А что можно сказать о лучевой диагностике заболеваний сердца?
– Достаточно часто применяется и конвенциональная коронарография стандартная, и КТ-коронарография, которая в последнее время приобретает большую распространённость в связи с появлением достаточно доступных контрастных веществ, вызывающих минимальное количество осложнений. Это относительно неинвазивный метод исследования, он более безопасен, чем другие методы, однако и у него есть ограничения, связанные с массой тела пациента, стадией заболевания, возрастом. Есть особенности в дифференциальной диагностике старых и новых бляшек в коронарных артериях, которые препятствуют кровотоку. Важно, активные они или неактивные. Поэтому метод для каждого пациента лучше подбирать индивидуально. Конвенциональная ангиография, стандартная коронарография тоже несёт риски, связанные с возможными повреждениями стенок сосудов, нарушением ритма сердца, повреждением клапанов. Всегда есть какой-то выбор, но, конечно, он обусловлен и тем, какими технологиями мы располагаем в каждой конкретной больнице. Говоря о радионуклидной диагностике, я снова вспоминаю замечательный рубидий-82, который получается из генератора, производимого в институте ядерных исследований. Он позволяет снизить лишнюю нагрузку на пациентов, как бы это ни было удивительно. Радионуклидная диагностика в этом случае подводит лучевую нагрузку примерно 4-5 миллизивертов от введённого препарата, в то время как КТ-коронарография подводит довольно большую дозу – порядка 16-18 миллизивертов. Плюс добавляются риски, связанные с контрастным веществом, которое может вызывать аллергические реакции. Обязательно нужно это учитывать. Радиофармацевтический препарат на основе рубидия не включается ни в какие физиологические процессы в теле человека. Он отражает перфузию миокарда, не влияет на организм и идеально всеми переносится. Более того, если у нас есть необходимость в визуализации конкретных бляшек, мы можем на компьютерном томографе параллельно с ПЭТ-исследованием провести коронарографию и получить красивую картинку, которая будет, с одной стороны, отображать перфузию миокарда, скорость миокардиального кровотока, фракционный резерв кровотока, а с другой стороны, на эту же картинку будет наложено изображение сосудов, где мы можем увидеть физическое существование бляшек: где они находятся, в какой артерии, в каком количестве.
Сопоставив эти данные гибридной визуализации, мы можем подобрать для каждого пациента максимально подходящую ему тактику лечения. Например, мы можем увидеть, что в одном из сосудов существует бляшка, которая препятствует кровотоку примерно на 50%, но, когда мы посмотрим результаты исследования, проведённого в нагрузке, мы увидим, что за счёт коллатералей, за счёт того сохранного кровотока, который функционирует, эта часть миокарда оказалась сохранна. Она перфузируется, там здоровые живые кардиомиоциты, они сокращаются. В этом случае нет необходимости проведения стентирования этого сосуда. Зато другой сосуд, который может обладать меньшим количеством коллатерального кровотока, требует обязательного вмешательства, в том числе, стентирования, шунтирования – для восстановления кровотока к участку миокарда, где кровоток снижен.
– Можно ли сказать, что будущее – за гибридными методами исследования, и мы постепенно отойдём от классических КТ и МРТ? Или все эти методы будут существовать параллельно?
– К каждому пациенту применима своя технология. Иногда можно обойтись рентгеном классическим, иногда нужно сделать КТ. Рентген при травме у маленьких детей желательно заменить компьютерной томографией, которая лучше выявляет переломы. Но иногда нам требуется применить дополнительные методы диагностики, и тогда мы переходим к уже более дорогим гибридным методам. Они займут свою нишу. У каждого метода диагностики будет своя ниша, и, думаю, если мы правильно организуем работу, правильно организуем общение врачей различных специальностей, будем хорошо готовить специалистов, то наши специалисты будут правильно выбирать методы диагностики и направлять пациентов на исследование. Иногда, к сожалению, получается, что исследования дублируются, пациентам дважды делают КТ в разных учреждениях, потому что что-то где-то не дописали, не пересмотрели. Если правильно организуем направление пациентов на нужное исследование, то всё будет хорошо, каждое исследование будет иметь свою нишу. Не скажу, что гибридные технологии заменят КТ. Они, скорее, будут его ощутимо дополнять.
– Получается, что для развития диагностических методов необходимо внимание уделить и образовательным программам?
– Обязательно. Именно поэтому я тоже работаю на кафедре лучевой диагностики и терапии Второго меда, стараюсь в меру своих сил помогать и в методической работе, в создании каких-то рекомендаций, стараюсь доносить до врачей, с которыми приходится работать, информацию о том, какие есть изменения, новшества. Я могу отметить очень много позитивных сдвигов: врачи стали лучше владеть английским языком, чаще обращаются к зарубежным рекомендациям, к стандартам лечения. Появляются и отечественные стандарты лечения – не медико-экономические стандарты, а то, что мы называем клиническими протоколами. Основаны содержащиеся в них рекомендации на большом объёме данных, связанных с клиническими исследованиями, проводимыми и в нашей стране, и за рубежом с вовлечением десятков тысяч пациентов. Это хороший базис доказательный медицины, который позволяет внедрять в практику новые технологии. И могу сказать, что уровень возрастает с каждым годом. Уже не нужно объяснять врачам, почему при лечении пациента с лимфомой необходимо иметь два исследования: до лечения и после него. Это нужно, чтобы оценить динамику. Все знают, что после второго, третьего курса терапии у пациента с лимфомой Ходжкина должно быть повторное КТ-исследование для оценки ответа.
– Что можете в качестве напутствия рассказать начинающим медикам, заинтересовавшимся радиологией?
– Какое напутствие? Вы будете много работать, будете не спать ночами, будете смотреть снимки. Станете настоящим “shadow geyzer” – разглядывателем теней, теневых изображений. Вы будете отлично разбираться в том, что видите. Будете видеть то, что происходит в глубине тела человека, то, что недоступно взгляду. Анатомию нужно очень хорошо учить и ни в коем случае не прогуливать. Если вы будете заниматься радионуклидной диагностикой, обязательно повторите курс паталогической физиологии, потому что очень многие процессы похожи друг на друга, их бывает достаточно сложно дифференцировать. Нужно обладать уверенными твёрдыми знаниями, никогда не заканчивать образование и вникать в различные процессы, которые происходят в теле человека. Смотреть, как же это будет выглядеть в рентгеновских лучах, думать о том, а что будет, если ввести сюда какой-нибудь краситель или препарат, меченный радиоактивным веществом, думать, как это поможет изучить какой-то интересный процесс, протекающий в теле человека.
Бывает, что в голове возникает вопрос по радионуклидной диагностике, мы открываем книжечку, а в ней написано, что всё, о чём мы сейчас думали, сделано ещё в 1960-е годы, задолго до нашей идеи. Не всегда есть вероятность открыть что-то новое, даже работая не в радиологии, а в других областях. То, что я рассказывал сегодня про болезнь Альцгеймера, про окрашивающие пигменты и вещества, которые используются в радионуклидной диагностике, идёт из патологической анатомии, из гистологии. Идея исходит оттуда.
– А что можете сказать о профдеформации? Имеет она место быть?
– Не могу сказать, что есть профдеформация. Просто периодически бывают случаи, когда я смотрю на изображение, вижу, что всё нормально, и хочется его побыстрее закрыть и описать, я понимаю, что есть вероятность какие-то моменты пропустить, не заметить. И в этом случае я прибегаю к технологии, которая применяется в нашей больнице – двойному пересмотру, когда исследование сначала кто-то описывает, а потом подходит второй врач и смотрит на это свежим взглядом. Мы стараемся пересматривать двумя парами глаз исследование. Если все в отпуске, то можно сделать заключение с вечера, а утром его ещё раз самому пересмотреть и поправить, если имеются, ошибки в протоколе. За рубежом часто исследование описывает резидент – грубо говоря, ординатор. Затем его верифицирует лечащий врач, и в конце недели все заключения попадают к заведующему отделения, который наделён многими полномочиями. Он их просматривает и тем, кто что-то пропустил, стучит по шапке. К сожалению, у нас это не всегда возможно. Мы работаем преимущественно с амбулаторными пациентами, которым нужно донести результаты до лечащего врача как можно скорее. И часто, вскакивая после обследования, пациент сразу хочет узнать его результат. Просим подождать. ПЭТ-исследования обрабатываются достаточно долго, стандартно включают в себя исследования зоны от основания черепа до середины бедра – это сканирование всего тела практически.
Как сообщалось ранее, порой ядерная физика работает на самую благородную цель — спасает человеческие жизни. Основное преимущество радионуклидной диагностики заключается в том, что с ее помощью можно поймать опасные патологические изменения еще на тех стадиях, когда их невозможно обнаружить традиционными методами визуализации. Подробнее читайте: Радиолог – о мифах КТ и ПЭТ: “Доктор, а мне нужно будет сжигать одежду?”